胫骨远端骨折三种内固定方式的有限元分析
王义昌 1 ,林文杰 2 ,林 涛 1 ,周柏安 1 ,黄文华 1,3 ,梁振明 1 ,魏劲松 1 ,欧阳汉斌 1
文题释义:骨折间隙微动:又称骨折间隙控制性细微的活动,是骨折愈合中重要的机械因素,有利于促进骨痂的生长,加快骨折愈合的速度。
有限元模型:是运用有限元分析方法建立的模型,是一组在节点处连接、仅靠节点传力、仅在节点处收约束的单元组合体。
摘要
背景:目前对比3种内固定技术治疗胫骨远端骨折生物力学特性差异的研究较少。
目的:比较胫骨远端骨折经胫骨内侧锁定钢板、专家级髓内钉和逆行髓内钉固定后生物力学特性的差异。
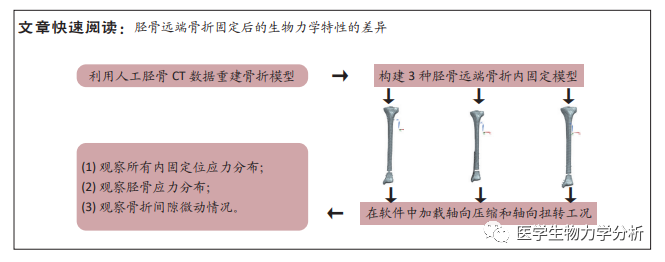
方法:基于SAWBONES第4代人工复合胫骨模型的CT数据,利用三维重建技术构建胫骨远端骨折数字模型(AO/ASIF 43-A3型),在此基础上模 拟胫骨内侧锁定钢板、专家级髓内钉和逆行髓内钉3种内固定方式;采用轴向压缩及扭转2种载荷工况分别对3组植入装配体模型进行有限 元分析,比较三者的应力分布、应力峰值及骨折间隙位移变化的差异。
结果与结论:①3组内固定物加载2种载荷工况时,专家级髓内钉组在扭转工况下应力峰值在未锁定的主钉孔处,为283.53 MPa;胫骨 内侧锁定钢板组在扭转工况下应力峰值位于第3颗螺钉上,为913.07 MPa;逆行髓内钉组在扭转工况下应力峰值在第2个主钉孔处,为 435.42 MPa;逆行髓内钉组内踝处主钉孔的周围皮质骨应力峰值出现在较高的轴向压缩工况下,峰值为55.34 MPa;②在骨折间隙位移方 面,加载轴向压缩载荷时,专家级髓内钉组4个区域的切向位移最高;胫骨内侧锁定钢板组4个区域的轴向位移最高,且峰值在外侧区;专 家级髓内钉组及逆行髓内钉组轴向位移峰值均位于后侧区;③加载轴向扭转载荷时,胫骨内侧锁定钢板组和逆行髓内钉组轴向位移峰值均 在外侧区,而逆行髓内钉组4个区域的切向位移均小于胫骨内侧锁定钢板组及专家级髓内钉组;④提示对于胫骨远端骨折,逆行髓内钉在 骨折端微动控制和内固定结构安全性方面相比胫骨内侧锁定钢板和专家级髓内钉更具优势。
关键词:内固定;胫骨远端骨折;有限元;生物力学;骨折间隙微动;应力分布
缩略语:胫骨内侧锁定钢板:medial distal tibial plate,MDTP;专家级髓内钉:expert tibial nail,ETN;逆行髓内钉:retrograde tibial nail,RTN
引言 Introduc■on
胫骨远端骨折约占成年人全身骨折的 1.5%[1]。随着交通 事故发生率逐年上升,流行病学研究发现,80% 的胫骨远端 骨折属于高能量损伤,由于胫骨远端皮肤薄、肌肉软组织覆 盖少、髓腔增宽等解剖形态特点,骨折后更容易出现感染、 骨折延迟愈合及骨不连等并发症 [1-2]。临床上胫骨远端干骺 端骨折常用的内固定方式主要有胫骨内侧锁定钢板 (medial distal ■bial plate,MDTP) 和专家级髓内钉 (expert ■bial nail, ETN)。然而,上述内固定存在一定的局限性,MDTP 术后常 出现骨不连和植入物感染 [3],ETN 术后可发生骨折对位、对 线不良及膝关节疼痛等并发症 [4]。为了兼顾骨折愈合生物学 和生物力学两方面因素,胫骨逆行髓内钉 (retrograde ■bial nail,RTN) 技术在 20 世纪 90 年代末由 HOFMANN 等 [5] 首次 提出,经过生物力学测试后,直到 2017 年在日本引入临床 实践中 [6],其采用内踝处作为进针点,在有效减少膝关节疼 痛发生的同时,能较好地保护局部软组织及骨膜的血供,以 更加接近骨折端的方式为干骺端骨折提供固定。目前关于 RTN 技术的生物力学研究仅有尸体力学实验研究,而对于胫 骨远端骨折不同内固定术式之间的力学性能差异尚无明确结 论,而 RTN 内固定对骨折微动和内踝应力的影响尚不明确。此次研究采用有限元方法,比较 MDTP、ETN 与 RTN 三种内 固定技术治疗胫骨远端骨折生物力学特性的差异,旨在为临 床手术方案选择提供更全面的生物力学依据。
1 材料和方法 Materials and methods
1.1 设计 三维有限元分析实验。
1.2 时间及地点 实验于 2021 年 9 月至 2022 年 5 月在广东 医科大学附属医院骨科数字骨科工作室和广东省医学 3D 打 印应用转化工程技术研究中心完成。
1.3 材料
1.3.1 实验对象 选用美国太平洋实验室生产的第 4 代人工 合成 Sawbones 胫骨模型 ( 编号:#3401),见图 1A。
 图注:图 A 为胫骨 sawbones 模型;
图注:图 A 为胫骨 sawbones 模型;
1.3.2 实验设备及软件 硬件设备:Dell T7910 图形工作站;64 排螺旋 CT(Siemens 公司,德国 );软件系统:Windows 10 专业版操作系统 (Microsoſt 公司,美国 ),医学图像三维重建 软件 Mimics 19.0(Materialise 公司,比利时 ),逆向工程建模 软件 Geomagic Studio 2013(Geomagic 公司,美国 ),CAD 辅 助设计软件 UG NX 10.0(Siemens 公司,德国 ),有限元分析 软件 Abaqus 2020( 达索 SIMULIA 公司,美国 )。
1.4 方法
1.4.1 胫骨远端骨折模型的建立 应用广东医科大学附属医 院 64 排螺旋 CT 逐层扫描 Sawbones 仿真胫骨模型,扫描层 厚和层间距均为 0.625 mm,获取 869 张断层 CT 图像,并以 DICOM(Digital Imaging and Communica■ons in Medicine) 格 式 导入到 Mimics19.0 软件中进行胫骨皮质骨和松质骨的三维几 何重建,以 STL 格式输出。将初步得到的胫骨三维模型导入 Geomagic Studio 2013 软件中,清除模型内部杂质并对表面 进行平滑修饰,进而运用精确曲面命令,完成胫骨皮质骨及 松质骨的实体化,保存为 STP 文件格式。进一步将构建的胫 骨皮质骨及松质骨实体模型导入到 NX.10.0 软件中,参照文 献报道的生物力学试验造模方法 [7],选取胫骨远端定义相应 的基准平面截取 10 mm 骨折间隙,模拟胫骨远端骨折 (AO/ ASIF 43-A3 型 ),见图 1B。
 B 为 AO/ASIF-43-A3 胫骨骨折模型;
B 为 AO/ASIF-43-A3 胫骨骨折模型;
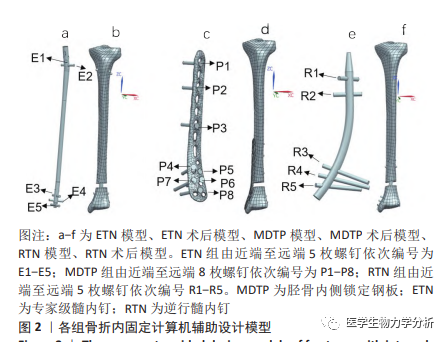
1.4.2 胫骨远端骨折内固定装配体模型的建立 由同一名高 年资骨科医师根据可视化胫骨模型尺寸分别选择相应规格 的 MDTP、ETN 和 RTN( 大博医疗科技股份有限公司 ),进而 对 3 种内固定物实物进行三维激光扫描 ( 设备:Goscan 三维 激光扫描仪 ),通过 Geomagic Studio 2013 软件进行点云数据处理和封装,并由该医师完成骨折模型及内固定物的初步装 配。进一步将初步装配后的骨折 - 内固定模型组以 STP 格式 导入 NX 10.0 中,根据厂家提供的螺钉几何参数,进行螺钉 的 CAD 模型设计及装配,最终完成 3 组胫骨远端骨折内固定 装配体模型组的建立 ( 图 2):① ETN 组 (B-MIN-01):髓内钉 长度 340 mm;主钉直径为 9.0 mm,锁定钉直径为 5 mm, 由近端至远端 5 枚螺钉依次编号为 E1-E5;② MDTP 组 (LCLP 10 胫骨远端内侧Ⅱ型 ):钢板厚度 3.65 mm,长度 160 mm;螺钉直径为 3.5 mm,由近端至远端 8 枚螺钉依次编号为 P1- P8;③ RTN 组 (A-MIN-01):髓内钉长度为 140 mm,主钉直 径为 8 mm,锁定钉直径为 4 mm,由近端至远端 5 枚螺钉依 次编号 R1-R5。此次研究对 3 种内固定螺钉的螺纹均进行几 何简化处理 [8]。
1.5 胫骨远端骨折内固定有限元模型的建立
1.5.1 材料赋值及网格划分 将 3 组内固定装配体模型导入 Abaqus 2020 有限元分析软件中,分别对皮质骨、松质骨和内 固定物进行材料赋值,材料参数参照既往研究均定义为均一 各向同性线弹性材料 [9-10],设置适合的弹性模量及泊松比 [11], 见表 1。模型组中钉 - 骨和钉 - 板界面采用绑定约束 [12]。进 一步对模型进行网格划分,单元网格类型为 C3D10,得到的 模型单元数量及节点数见表 2。

 1.5.2 载荷工况及边界条件 参照以往实体试验 [13],加载由 低到高的非破坏性载荷的方法,选取轴向压缩工况及轴向扭 转工况以模拟正常人体行走时胫骨承受的主要载荷类型:① 轴向压缩工况:以胫骨的力线轴作为局部坐标系中 X 轴, 对胫骨平台施加大小为 350 N 及 600 N 的轴向压缩载荷,胫 骨平台内、外侧关节面分别承受 60% 及 40% 的力 [14],见图 1C;②轴向扭转载荷工况:沿胫骨力线轴分别施加 3 Nm 及 8 Nm 的轴向扭转载荷,见图 1C。所有工况均约束胫距关节 上关节面单元节点的 6 个方向自由度 [15]。
1.5.2 载荷工况及边界条件 参照以往实体试验 [13],加载由 低到高的非破坏性载荷的方法,选取轴向压缩工况及轴向扭 转工况以模拟正常人体行走时胫骨承受的主要载荷类型:① 轴向压缩工况:以胫骨的力线轴作为局部坐标系中 X 轴, 对胫骨平台施加大小为 350 N 及 600 N 的轴向压缩载荷,胫 骨平台内、外侧关节面分别承受 60% 及 40% 的力 [14],见图 1C;②轴向扭转载荷工况:沿胫骨力线轴分别施加 3 Nm 及 8 Nm 的轴向扭转载荷,见图 1C。所有工况均约束胫距关节 上关节面单元节点的 6 个方向自由度 [15]。
 C 为胫骨加载轴向压缩及扭转载荷的方向和 Abaqus 中空间坐标系 xyz;
C 为胫骨加载轴向压缩及扭转载荷的方向和 Abaqus 中空间坐标系 xyz;
1.6 主要观察指标 将完成前处理的 3 组有限元模型提交至 Abaqus Standard 求解器中进行分析,观察不同工况条件下 3 组模型的 von Mises 应力分布、应力峰值及不同位置上的骨 折端位移变化差异。骨折间隙位移用近端骨折块内侧皮质骨 上 24 个节点的位移曲线来表示,将 24 个节点划分为骨折间 隙的前、后、内、外侧区域,见图 1D。
 D 为近端骨折块下面观,24 个节点,顺时针编号,1-6 为前侧,7-12 为 外侧,13-18 为后侧,19-24 为内侧
D 为近端骨折块下面观,24 个节点,顺时针编号,1-6 为前侧,7-12 为 外侧,13-18 为后侧,19-24 为内侧
2 结果 Results
2.1 模型有效性验证 参照既往力学试验文献的加载条件, 计算低轴向压缩工况中 3 组有限元模型的整体结构刚度, MDTP 组 为 613.04 N/mm,RTN 组 为 827.43 N/mm,ETN 组 为 603.01 N/mm。与既往实体试验相比 [16-17],ETN 组 为 (888± 249) N/mm,RTN 组 为 (609±149) N/mm,MDTP 组 为 (465± 178) N/mm。总体上结果较为相近,证明了该有限元模型的 有效性。
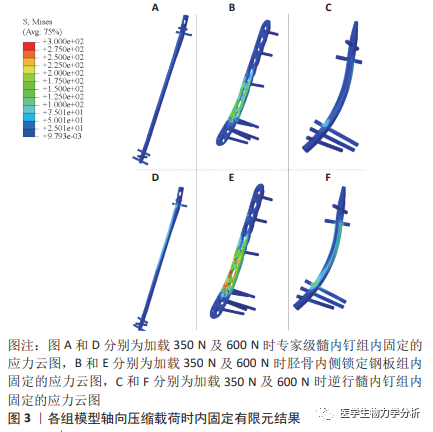
2.2 不同工况中 3 种内固定物应力分布及应力峰值 在轴向 压缩工况中,3 个模型组内固定物的应力分布云图,见图 3。可以看出,分别施加 350 N 和 600 N 压缩载荷时,ETN 组内固定高应力区主要位于 E2 主钉孔处,应力峰值分别为 156.73 MPa 和 269.06 MPa;MDTP 组内固定高应力区主要位 于 P3 螺钉上,应力峰值为 430.62 MPa 和 737.78 MPa;在 RTN 组内固定高应力区则位于 R3 螺钉上,应力峰值分别为 145.81 MPa 和 242.67 MPa。
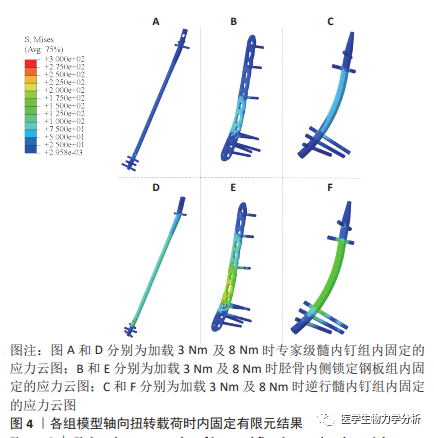
在轴向扭转工况中,3 个模型组内固定物的应力分布 云图,见图 4。加载扭转 3 Nm 及 8 Nm 载荷时,ETN 组内固定物的高应力区出现在骨折间隙间中未锁定的主钉孔内 上,应力峰值分别为 106.31 MPa 及 283.53 MPa;对于 MDTP 组,内固定的高应力区集中在 P3 螺钉上,应力峰值分别为 450.27 MPa 及 913.07 MPa;RTN 组在内固定的高应力区集 中在 R2 螺钉的主钉孔上,应力峰值分别为 163.54 MPa 及 435.42 MPa。
2.3 不同工况中 3 组模型胫骨应力分布及应力峰值 在轴向 压缩工况中,3 个模型组胫骨的应力峰值,见表 3。在加载 350 N 及 600 N 载荷时,ETN 组胫骨高应力区在 E2 内侧钉孔 周围的皮质骨;MDTP 组的胫骨高应力区在 P4 内侧钉孔周围的皮质骨;RTN 组胫骨高应力区在 R3 内侧钉孔周围的皮质 骨。在轴向扭转工况中,3 个模型组胫骨的应力峰值,见表 3。加载 3 Nm 及 8 Nm 扭转载荷,ETN 组胫骨的高应力区也 在 E2 钉孔外侧周围的皮质骨上;MDTP 组中胫骨的高应力区 为 P3 螺钉孔内侧周围的皮质骨;RTN 组中胫骨高应力区在 R3 钉孔内侧周围皮质骨。
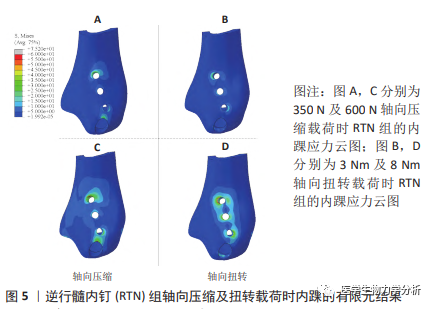
2.4 RTN 内固定下内踝处骨骼的应力分布 RTN 组内踝处 的应力分布,见图 5。在 2 种轴向压缩载荷时,内踝主 钉孔周围皮质骨高应力区靠近骨折端,应力峰值分别为 32.66 MPa 及 55.34 MPa。RTN 组 2 种扭转载荷下主钉孔周 围皮质骨高应力区靠近踝关节面,应力峰值为 10.56 MPa 及 26.92 MPa。
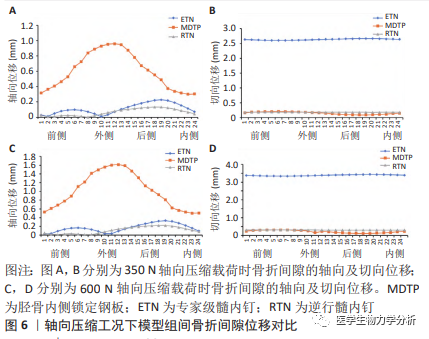
2.5 不同工况下 3 组模型组间的骨折间隙位移 在轴向压缩 工况下,对比 3 组内固定模型的骨折间隙轴向位移结果,见 图 6。MDTP 组所有区域均明显大于 ETN 及 RTN 组,MDTP 组轴向位移**值在外侧区,为 1.62 mm;ETN 组及 RTN 组 则位于后侧区,为 0.33 mm 及 0.22 mm。对比 3 组内固定模 型的骨折间隙切向位移结果可以发现,ETN 组所有区域均明 显大于其他两组模型,MDTP 及 RTN 骨折间隙切向位移基本 一致,而 MDTP 组后内侧区位移要略低。
在轴向扭转工况下,对比3组内固定模型的骨折间隙轴向位 移结果,见图 7。MDTP 组位移**值位于前侧区,为 0.13 mm; ETN 组位于外侧区,为 0.01 mm;RTN 组则位于前侧区,为 0.04 mm。对比 3 组内固定模型的骨折间隙切向位移结果, MDTP 及 ETN 组在外侧区的位移值**,分别为 1.73 mm 及 0.84 mm;RTN 组位移**值则位于外侧区,为 0.42 mm。

3 讨论 Discussion
胫骨远端解剖位置较为特殊,具有周围软组织覆盖少、周 围血运较差和比邻踝关节等解剖特点,不同的内固定方式对不同 的骨折类型术后稳定性的影响也不尽相同。手术方式的选择需要 临床医师综合的判断,目前临床上主要采用 MDTP 或 ETN 内固 定治疗AO/ASIF 43-A3 型骨折 [18-19]。有研究显示,胫骨远端皮肤 完整者可以考虑经皮或有限切开应用 MDTP 内固定术 [20],相比 ETN 可减少内固定术后对线不良的问题 [21]。BAHAMONDE 等 [22] 认为与 MDTP 相比较,ETN 术中扩髓处理后,髓内骨屑“内植骨 效应”有利于降低术后愈合不良的并发症发生率,同时有限的软 组织破坏还能减少术后感染发生率。尽管如此,扩髓处理同样会 增加脂肪栓塞的风险 [23]。近年来,为克服传统 MDTP 或 ETN 上 述固有的并发症问题,有学者提出应用 RTN 内固定治疗胫骨远 端骨折,但该内固定系统的生物力学研究仍局限在传统的尸体标 本力学实验,而实验更无法观察到胫骨及内固定物的内部应力分 布情况 [24]。当前,医学有限元分析技术已被广泛运用于骨科生物 力学研究领域 [25-27]。因而,此次研究利用有限元分析技术对 RTN内固定的生物力学特性进行评价,并与传统内固定系统进行对比 研究,为 RTN 在临床应用方面的安全性和有效性提供更有力的 生物力学理论依据。
此次研究就 3 种内固定系统在同等载荷条件下表现出 来的结构刚度进行了对比分析,结果显示 RTN 的轴向刚度 要显著优于 MDTP 和 ETN 组。而在此前的系列研究中,对于 固定后整体结构刚度方面,RTN 相比髓外固定系统也同样表 现出髓内固定固有的力学优势,和此次研究结论相一致 [5]。 值得注意的是,RTN 由于是经内踝逆行置钉,对于胫骨远端 骨折的工作长度相比顺行 ETN 的工作长度更短,因此固定刚 度更高;同样,髓外固定的 MDTP 具有近似的工作长度,由 于偏心固定 [28-29],其轴向刚度显著低于 RTN。除此以外,骨 折愈合还受骨折间隙微动因素的影响 [30]。此次研究对 3 组 模型固定下的骨折断端微动进行了对比分析,MDTP 固定骨 折端的轴向微动水平最高,而 RTN 的轴向微动则总体略低 于 ETN,体现了髓内固定对轴向微动的控制具有明显优势, 尽管这一优势在骨折愈合的中后期逐渐弱化。而对于轴向 压缩载荷下的切向微动,RTN 和 MDTP 均表现较低的微动水 平,主要原因在于 ETN 相比上述二者较短的工作长度,远 离骨折端的交锁螺钉未能较好控制切向位移。而 NOURISA 等 [31] 的研究同样指出,在加载轴向压缩载荷时,ETN 组骨 折块间隙的切向位移明显大于 MDTP 组,此次研究结果与 之一致。骨折间隙较低的轴向微动及过度的切向微动不利 于骨痂中血管的形成,更不利于骨痂塑形和矿化 [32]。EPARI 等 [33] 则认为切向微动结合轴向微动不会影响骨折愈合,然 而,切向及轴向微动水平的比例尚无明确的结论。SCHELL 等 [34] 认为切向与轴向微动比值小于 2 是安全的。而此次研 究中,ETN 组骨折间隙的切向与轴向微动比值均大于 2,反 观 MDTP 组及 RTN 组相应的该比值则明显小于 2,故 ETN 组 未能提供相应的力学优势。既往文献显示,骨折间隙过大 的切向微动易造成 ETN 术后继发性对线不良,甚至延迟愈 合 [30]。就胫骨下段沙漏状髓腔特点来看,ETN 固定会导致骨 折间隙过多的切向微动,而 RTN 可减少这种微动,具有一定 优势。与此同时,作者发现 MDTP 组骨折间隙的轴向及切向 微动在靠近钢板固定侧时都明显下降, 而 ETN 及 RTN 表现 较为均匀,不难推测 MDTP 骨折间隙的非对称微动也可能会 影响骨痂愈合质量。ETN 术后早期负重行走得益于术后较高 的轴向刚度 [17],此次研究中 ETN 的轴向刚度略小于 RTN,该 结论与 KUHN 等 [6] 的研究结论一致。因此,较高的轴向刚度 和骨折间隙低水平的切向微动使得 RTN 术后允许早期负重。
胫骨远端 RTN 经内踝逆行置钉的优势在于把固定物的 把持部位带到骨折附近,显著提升了力学稳定性,然而,经 内踝置钉有降低局部骨质强度的风险,进而增加术后医源性 骨折的风险。此次研究进一步对内踝皮质骨的应力强度进行 分析,结果显示 RTN 内踝主钉入口周围并无显著的应力集中, 且应力峰值不超过 60 MPa;不仅如此,ETN 及 RTN 组在内踝 钉孔周围的皮质骨应力峰值均明显小于 MDTP 组,基本符合临床上观察到的多数病例 ETN 及 RTN 术后恢复前期,内踝的 不适感较少 [35-36]。除内踝处应力分布情况外,RTN 组模型中 内固定物及胫骨的应力峰值大部分都集中在 R2 和 R3 螺钉周 围,MDTP 组及 ETN 组内固定峰值都在最靠近骨折间隙的锁 定钉上,与 BASERI 等 [37] 的研究结果一致。KUHN 等 [7] 认为 RTN 可能的适应证是胫骨远端骨折 (AO/ASIF 42A-C 型、AO/ ASIF 43A1-3 型 ),以及结合附加螺钉固定的单纯性 Pilon 骨 折 (AO/ASIF 43C1)。此次研究在干骺端构建 10 mm 的缺损模 拟 AO/ASIF 43A3 型粉碎性骨折模型,以证明 RTN 在该骨折 类型的生物力学优越性。在临床上,何敏等 [36] 回顾性分析 了 RTN 治疗胫骨远端骨折 (AO/ASIF 43A1-3 及 AO/ASIF 43C1-2 型 ) 的病例,均达到临床愈合,且无并发症的发生,踝关节 AOFAS 评分均为优良,与 PENG 等 [38] 的研究结果一致。
此次研究尚有一定的局限性:首先,此次研究所用的 SAWBONES 胫骨模型虽然克服了个体化差异,但仅能代表普 通健康成人的骨质条件[39],无法得到骨质疏松条件下的结论; 其次,此次研究仅仅模拟了日常生活中比较具有代表性的工 况条件,生理条件下患者的力学环境更是一个动态的作用过 程,实际载荷参数更为复杂 [40-41],由于骨折缺损处过于靠近 干骺端,故此次研究未加载侧向载荷进行三点或四点弯曲试 验。尽管如此,此次研究中的有限元分析建模提供了等参条 件下的模型对比数据,能够更为有效地控制计算结果的准确 度和稳定性,具有较高的说服力。
综上,RTN 在治疗胫骨远端骨折 (AO/ASIF 43-A3 型 ) 是 一种安全有效的固定方式,尤其在骨折微动控制和应力分布 方面,相比传统 ETN 和 MDTP 具有明显的优势。
转载自:医学生物力学分析
免责声明:本文系网络转载或改编,版权归原作者所有。如涉及版权,请联系删